通过使两个Cas9核酸酶域中的一个发生突变,研究人员创造了CRISPR nickase。Nickases产生单链而不是双链断裂,当与两个相邻的gRNAs一起使用时,可以降低脱靶编辑的概率。在这篇文章中,我们将总结IDT(集成DNA技术)是如何首次演示CRISPR nickases如何改进的同源性定向修复价格,并分享他们的设计规则,为您的下一个CRINPR酸切除酸味实验
Cas9 nickase概述
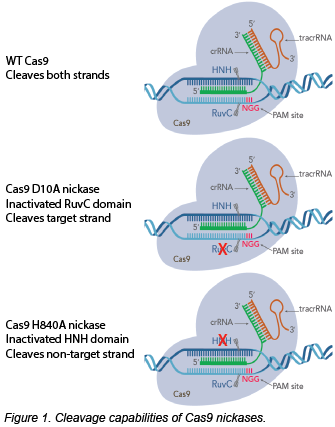
我们将使用SPCAS9 inckase作为此帖子的示例。D10A突变灭活ruvc结构域,因此该酸酶仅切割目标链。相反,H840a在HNH结构域中的突变产生非靶链裂解乳糜序列。而不是用WT Cas9和一个GRNA钝密地切割两条链,而是可以使用Cas9缩乳和两个GRNA产生交错的切割。
对于nickase的应用,一个常见的问题是:在比较中,gRNAs应该如何定向?gRNAs必须针对不同的链来创建DSB,但这可以通过PAM-in或PAM-out定向来完成。顾名思义,PAM-out设计将PAM序列放在目标区域的极端位置,而PAM-in设计将PAM序列放在目标区域的中间位置,如下图所示。

为了确定最佳镍酶设计,IDT的科学家Mollie Schubert和Shuqi Yan设计了使用HEK293细胞测试镍酶偏好的实验。他们首先比较了D10A和H840A在不同缺口距离(40 - 130nt)下PAM-in和PAM-out配置中的总编辑效率。从这些结果中可以清楚地看出,在PAM-out配置中,编辑要高得多。此外,D10A的编辑效率始终高于H840A,尤其是在缺口距离较小的情况下。利用D10A,他们随后发现,当gRNAs过于接近(7-23 nt nick distance)时,编辑效率非常低。
D10A和H840A都是有效的编辑器,但它们的indel谱有所不同。在PAM-out配置中,D10A倾向于产生小的缺失,而H840A倾向于产生大的插入。这些剖面可能是由于由nickases产生的不同的突出模式;在PAM-out设计中,D10A创建5 '悬挑,H840A创建3 '悬挑。
探索同源性定向修复的乳酸
使用nickase的潜在好处HDR目标范围:使用单独的gRNA与WT Cas9,维修水平从切割点迅速减少10磅。因此,如果您无法找到靠近插入网站的良好GRNA,则无法获得高HDR效率。尼克加斯创造了一个交错的切割 - 这个系统可以在缺口之间的整个地区修复修复吗?要查明,Schubert和Yan设计了一种PAM-Out Nickase实验,以使用单链寡核苷酸(SSODN)供体插入ECORI位点。使用D10a Nickase将ECORI位点插入缺口部位之间的各种斑点,使用具有40bp同源臂的顶部或底部链SSODN供体在51个NT区域上观察> 20%的修复(最多27%)。HDR效率有利地使用WT Cas9在窗口上使用左GRNA。在随后的实验中,它们还能够使用具有100nT同源臂的IDT MEGAMER LONG SSDNA引入更长的插入(MCHERRY)。

舒伯特和Yan接下来研究了一种被认为对HDR不是最优的情况。在AAVS1.轨迹,两个最接近的GRNA有切割位点12nt和13 nt远离目标位点而不是最佳<10nt距离。使用两种远离靶位点的GRNA位点,它们设计了D10A = Quidase策略(46 NT刻度距离,PAM-OUT),以查看它们是否可以解决这个问题。D10A Nickase优于通过宽边缘测试的WT Cas9位点,表现出> 20%的修复效率。显然,尼氨酶策略可以扩展可靶区域,如果没有接近所需的突变位点的可用引导件,则特别有用。

nickase设计的快速提示
准备好在你的下一次CRISPR实验中使用nickes了吗?以下是IDT的最佳建议:
- 使用PAM-out配置
- 优化你的间距
- D10A:分隔的尼克网站(BP)
- H840A:缺口位点,间隔51-68 bp
- 对HDR使用D10A
- 在刻痕位置之间放置预定的插入物
- 使用40个NT同源臂进行小插入或标签(SSODN;IDTUltramer®寡核苷酸的)
- 使用100 NT同源臂进行大插入(长SSDNA;IDTMegamer®SSDNA碎片的)
- 测试底部和顶部链SSDNA供体(如果可能的话)
本文中的文字和图片改编自IDT网络研讨会:在基因组编辑中使用Cas9 nickases的优化方法。欲了解更多信息并链接到已存档的网络研讨会,点击这里。我们要感谢IDT科学家Mollie Schubert和Shuqi Yan进行审查。
addgene博客上的其他资源188博金宝官网
addgene.org的资源
- 查看CRISPR主题页面
- 找到CRISPR酸氨酶质粒
- 浏览CRISPR指南








留下你的评论